Glossaire PCM 1ère
Spécial | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | Tout
A |
|---|
accélérationLe vecteur accélération est un vecteur dont les coordonnées : - sont les fonctions dérivées des coordonnées du vecteur-vitesse, donc les dérivées secondes de celles du vecteur-position : \( \displaystyle a_x=\frac{d v_x}{dt}= \frac{d^2 x}{dt^2} \ ; \ a_y=\frac{d v_y}{dt}= \frac{d^2 y}{dt^2} \ ; a_z=\frac{d v_z}{dt}= \frac{d^2 z}{dt^2} \) soit : \( \displaystyle \overrightarrow{a} = \frac{d \overrightarrow{v}}{dt} = \frac{ d^2\overrightarrow{OM}}{dt^2} \) - ont des valeurs exprimées en \( \mathrm{m\cdot s^{-2}} \) | |
C |
|---|
céléritéLa célérité est le nom donné à la vitesse de propagation d'une onde. Son unité SI est le \( \mathrm{m\cdot s}^{-1} \). | |
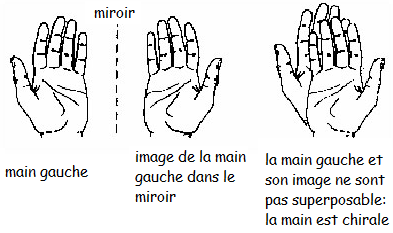
chiralitéLa chiralité est la propriété d'un objet qui n'est pas superposable à son image dans un miroir.
Une molécule qui possède un atome de carbone lié à quatre groupes tous différents est forcément chirale. Exemple :
Ces deux molécules ne sont pas superposables : elles sont chirales toutes les deux. | ||
chute libre | |
É |
|---|
électronégativitéL'électronégativité est une grandeur sans dimension qui traduit la capacité d'un atome à attirer
les électrons lors de la formation d'une liaison chimique. Elle évolue ainsi au sein du tableau périodique :
C'est la différence d’électronégativité des deux atomes liés qui explique que certaines liaisons chimiques soient polaires. | ||
énantiomérieL'énantiomérie est une relation entre deux molécules. Deux molécules non superposables et images l'une de l'autre dans un miroir forment un couple d'énantiomères.
Ces deux molécules sont énantiomères l'une de l'autre. | ||
énergie cinétiqueL'énergie cinétique est l'énergie stockée par un système du fait de son mouvement. Elle vaut : \( \displaystyle Ec = \frac{1}{2} m v^2 \) \( Ec \) étant exprimée en joule (J), \( m \) en kg et \(v\) en m·s–1. | |
F |
|---|
facteur cinétiqueUn facteur cinétique est une grandeur physique ou chimique dont la valeur a une influence sur la vitesse de la réaction chimique. Deux exemples de facteurs cinétiques : la température et la concentration des réactifs. | ||
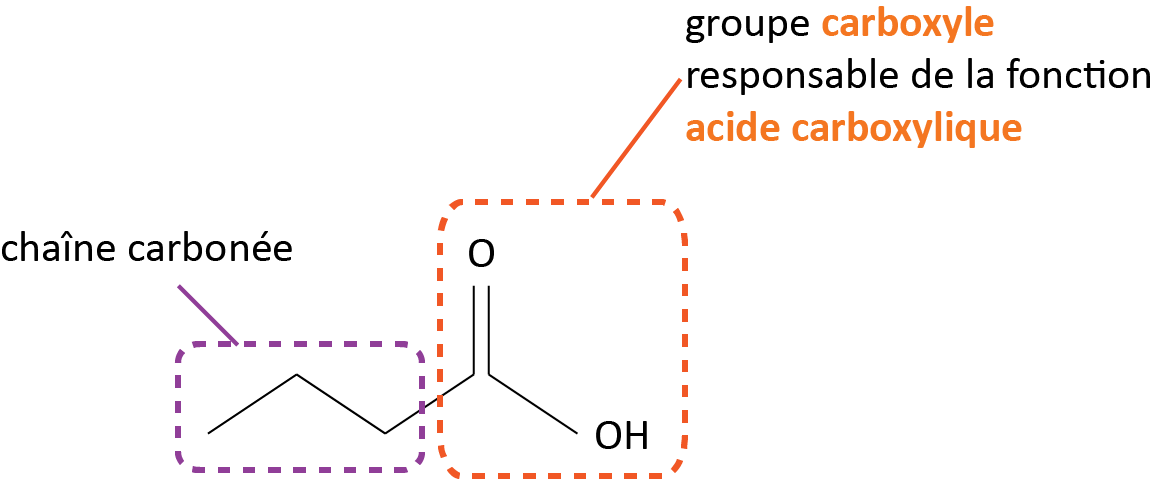
fonction chimiqueUne molécule organique possède : - une ou plusieurs chaînes carbonées, constitués d'atomes de carbone et d'hydrogène liés par des liaisons simples. La chaîne carbonée influe principalement sur les propriétés physiques. - d'un ou plusieurs groupes caractéristiques (liaisons multiples, atomes autres que C et H), qui influent sur les propriétés physiques et chimiques de l'espèce considérée. Chaque groupe caractéristique confère à une molécule une fonction chimique. Exemple de l'acide butanoïque :
| ||